發(fā)布時(shí)間:2023-09-23
9月22日,中國科學(xué)院廣州生物醫(yī)藥與健康研究院李鵬團(tuán)隊(duì)和劉興國團(tuán)隊(duì)共同在國際學(xué)術(shù)期刊EMBO Journal上發(fā)表了題為“BCL11B and the NuRD complex cooperatively guard T-cell fate and inhibit OPA1-mediated mitochondrial fusion in T cells”的研究成果,揭示了人成熟T細(xì)胞中BCL11B可與NuRD復(fù)合物相互作用直接抑制NK細(xì)胞相關(guān)基因轉(zhuǎn)錄,還可間接通過代謝-表觀遺傳軸維持T細(xì)胞命運(yùn)。
過繼性細(xì)胞免疫療法已成為放化療之后的又一種有效控制腫瘤的手段。近年來,嵌合抗原受體(Chimeric Antigen Receptor, CAR)T細(xì)胞作為過繼性細(xì)胞療法的代表,對(duì)血液腫瘤表現(xiàn)出強(qiáng)勁的抗腫瘤效果,但在實(shí)體瘤的治療上仍不盡人意。優(yōu)化、改造免疫細(xì)胞是提高實(shí)體瘤的免疫治療的新策略。李鵬團(tuán)隊(duì)前期研究發(fā)現(xiàn),通過CRISPR/Cas9系統(tǒng)敲除人成熟T細(xì)胞中BCL11B可誘導(dǎo)其重編程為類NK細(xì)胞(induced T-to-natural killer cells,ITNK細(xì)胞)。ITNK細(xì)胞同時(shí)具有T細(xì)胞和NK細(xì)胞的表型和功能特征。在體內(nèi)外具有更廣譜和更強(qiáng)效的抗實(shí)體瘤活性。初步臨床實(shí)驗(yàn)(NCT:03882840)結(jié)果也表明,患者自體誘導(dǎo)的 ITNK 細(xì)胞對(duì)復(fù)發(fā)難治的晚期實(shí)體瘤有一定療效且不會(huì)引起任何嚴(yán)重不良反應(yīng)。因此 ITNK 細(xì)胞可作為一種新的細(xì)胞來源用于腫瘤免疫治療,但其強(qiáng)效抗腫瘤活性的分子機(jī)制仍不清楚。
本項(xiàng)研究發(fā)現(xiàn)BCL11B可直接與NuRD復(fù)合物關(guān)鍵亞基相互作用,抑制T細(xì)胞中NK相關(guān)基因的表達(dá)。敲除NuRD復(fù)合物關(guān)鍵亞基,包括MBD2、MTA2和CHD4均可將人成熟T細(xì)胞重編程為ITNK細(xì)胞,這些ITNK細(xì)胞與敲除BCL11B來源的ITNK細(xì)胞具有相似的轉(zhuǎn)錄本和抗腫瘤活性,為獲得ITNK細(xì)胞提供了新的來源。
細(xì)胞代謝可影響T細(xì)胞的分化狀態(tài)和功能。本研究發(fā)現(xiàn),在T細(xì)胞中BCL11B可直接結(jié)合在線粒體內(nèi)膜融合蛋白視神經(jīng)萎縮1(optic atrophy1,OPA1)基因的TSS區(qū)并抑制其轉(zhuǎn)錄,敲除BCL11B可上調(diào)表達(dá)OPA1并介導(dǎo)線粒體融合。融合線粒體促進(jìn)了ITNK細(xì)胞氧化磷酸化(OXPHOS)代謝水平,進(jìn)而促進(jìn)ITNK細(xì)胞重編程效率和抗腫瘤活性。代謝產(chǎn)物不僅可以作為代謝信號(hào)調(diào)控細(xì)胞生物大分子合成為細(xì)胞提供物質(zhì)和能量,還可作為非代謝信號(hào),通過組蛋白或DNA表觀修飾調(diào)控基因表達(dá)。本研究進(jìn)一步發(fā)現(xiàn)ITNK細(xì)胞OXPHOS代謝增強(qiáng)乙酰-CoA水平,高濃度的乙酰-CoA作為組蛋白乙酰化的底物,通過增加NK相關(guān)基因及細(xì)胞毒性相關(guān)基因位點(diǎn)的H3K27乙酰化修飾,促進(jìn)相關(guān)基因的表達(dá),提升ITNK細(xì)胞的抗腫瘤活性。
本項(xiàng)研究揭示了轉(zhuǎn)錄因子BCL11B在T細(xì)胞代謝中的重要作用,豐富了 BCL11B在T細(xì)胞中的生物學(xué)意義。同時(shí),通過解析ITNK細(xì)胞的代謝-表觀遺傳軸,揭示了代謝重塑通過組蛋白表觀修飾調(diào)控ITNK細(xì)胞抗腫瘤活性的分子機(jī)制,為進(jìn)一步提升ITNK細(xì)胞臨床治療實(shí)體瘤效果提供了新策略。
中國科學(xué)院廣州生物醫(yī)藥與健康研究院博士后廖芮、副研究員鄔毅為該論文的共同第一作者。中國科學(xué)院廣州生物醫(yī)藥與健康研究院李鵬研究員、劉興國研究員為本論文的共同通訊作者。該研究成果得到國家重點(diǎn)研發(fā)計(jì)劃、國家自然科學(xué)基金等項(xiàng)目的資助。
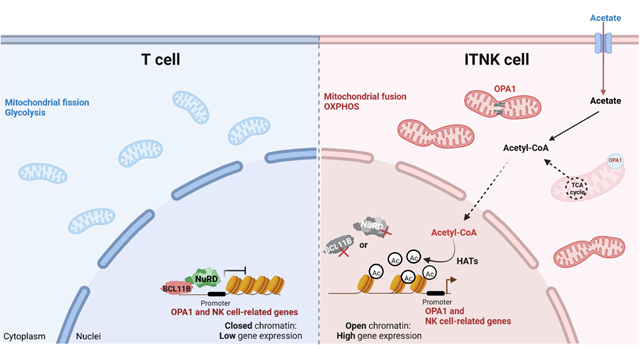
BCL11B與NuRD復(fù)合物共同調(diào)控T細(xì)胞命運(yùn)的機(jī)制研究示意圖
附件下載:

