發(fā)布時(shí)間:2024-01-15
近日,中國科學(xué)院廣州生物醫(yī)藥與健康研究院潘光錦團(tuán)隊(duì)在Stem Cell Reports期刊發(fā)表了題為“Autophagy is essential for human myelopoiesis”的文章。該研究揭示了ATG7依賴的自噬調(diào)控人粒系祖細(xì)胞在緊急粒細(xì)胞分化過程中擴(kuò)增的作用機(jī)制。
粒細(xì)胞是人體內(nèi)一類重要的免疫細(xì)胞,在感染免疫、炎癥調(diào)控及腫瘤發(fā)生等方面均發(fā)揮重要作用。當(dāng)面對(duì)系統(tǒng)性感染時(shí),人體啟動(dòng)緊急粒細(xì)胞分化(Emergency myelopoiesis,EM)程序,粒系祖細(xì)胞(myeloid progenitors,MPs)迅速擴(kuò)增,產(chǎn)生大量粒細(xì)胞抵抗病原體,保護(hù)人體健康。然而,在EM過程中,調(diào)控MPs擴(kuò)增的具體機(jī)制尚知之甚少。研究報(bào)道,自噬在小鼠粒細(xì)胞發(fā)育過程中扮演著重要角色,而由于倫理和取材的限制,自噬對(duì)人粒細(xì)胞分化擴(kuò)增調(diào)控的研究相對(duì)較少。因此,研究團(tuán)隊(duì)基于前期開發(fā)的人多能干細(xì)胞(human pluripotent stem cells,hPSCs)體外造血分化體系,在體外建立了EM模型,并進(jìn)行了深入探究。
研究團(tuán)隊(duì)在人動(dòng)員外周血來源的造血干/祖細(xì)胞(hematopoietic stem/progenitor cells,HSPCs)及hPSCs來源的HSPCs中,分別對(duì)自噬關(guān)鍵基因ATG7進(jìn)行了敲降或敲除,隨后利用體外EM模型進(jìn)行了探究。研究表明,自噬缺陷的MPs在EM過程中伴隨顯著的擴(kuò)增障礙,而只有過表達(dá)可回補(bǔ)自噬功能的全長型ATG7,而非突變型ATG7,才可恢復(fù)ATG7-/--HSPCs來源MPs在EM過程中的擴(kuò)增能力。這些結(jié)果說明ATG7通過其自噬依賴的功能維持MPs在EM過程中的擴(kuò)增能力。
接下來,研究團(tuán)隊(duì)發(fā)現(xiàn)自噬缺陷的MPs中堆積了大量的p53蛋白,而p53的mRNA卻沒有顯著上調(diào),提示自噬可能通過調(diào)控p53蛋白的穩(wěn)定性來發(fā)揮重要作用。隨后,研究團(tuán)隊(duì)利用Co-IP技術(shù),在MPs中檢測(cè)到了p53蛋白與自噬底物銜接蛋白LC3B的互作,表明p53可作為自噬的降解底物。進(jìn)一步的結(jié)果顯示,自噬缺陷顯著降低了MPs中p53蛋白和自噬下游重要細(xì)胞器-溶酶體的共定位,說明自噬的缺陷導(dǎo)致被運(yùn)送至溶酶體中進(jìn)行降解的p53蛋白變少了,進(jìn)一步驗(yàn)證了p53蛋白被自噬-溶酶體途徑降解的機(jī)制。而且,在自噬缺陷的MPs中敲降p53后,可顯著恢復(fù)MPs在EM過程中的擴(kuò)增能力。
綜上,該研究表明了ATG7依賴的自噬通過降解p53蛋白,釋放MPs的增殖能力,從而保障了MPs在EM過程中的擴(kuò)增。該研究為理解人粒細(xì)胞的分化擴(kuò)增調(diào)控提供了新的見解,并為臨床開發(fā)治療粒細(xì)胞白血病的方法提供了潛在靶點(diǎn)。
廣州健康院博士后谷佳明、副研究員朱艷玲為該論文的共同第一作者。廣州健康院潘光錦研究員為該論文的通訊作者。該研究成果得到了國家重點(diǎn)研發(fā)計(jì)劃、國家自然科學(xué)基金等項(xiàng)目的資助。
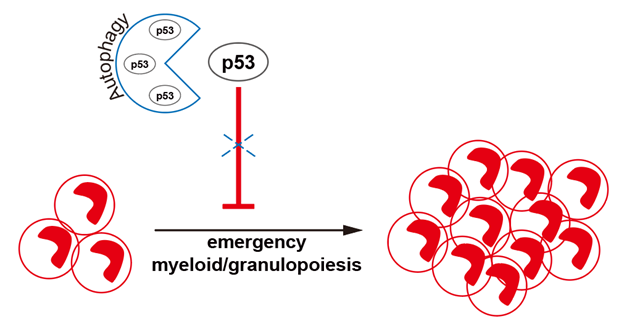
自噬調(diào)控人粒系祖細(xì)胞中p53降解的示意圖
附件下載:

