發(fā)布時間:2024-04-26
近日,中國科學(xué)院廣州生物醫(yī)藥與健康研究院許永研究員課題組報道了一種新型的、高效的靶向CBP/p300的PROTAC降解劑,可用于治療急性髓系白血病(Acute myeloid leukemia,AML)。相關(guān)成果近日以“Discovery of Highly Potent and Efficient CBP/p300 Degraders with Strong In Vivo Antitumor Activity”為題發(fā)表在美國化學(xué)會(ACS)Journal of Medicinal Chemistry上。
AML是常見的血液惡性腫瘤之一,嚴(yán)重威脅患者的生命健康。AML患者的五年總生存率低于40%,而且發(fā)病率隨著年齡的增長而增加。因此,臨床上亟需開展基于新靶標(biāo)、新機制的抗AML藥物研究。
環(huán)磷酸腺苷反應(yīng)元件結(jié)合蛋白(CREB)結(jié)合蛋白(CREBBP,CBP)及其高度同源的腺病毒EA1結(jié)合蛋白(EP300,p300)作為轉(zhuǎn)錄共激活因子與AML的發(fā)生發(fā)展密切相關(guān)。近20多年來,許多CBP/p300小分子抑制劑被報道。其中,CellCentric公司開發(fā)的CCS1477率先進(jìn)入臨床1/2期研究,用于白血病、前列腺癌等癌癥的治療。然而,目前還沒有相關(guān)藥物上市。
許永團(tuán)隊長期致力于CBP/p300小分子抑制劑的研究,并獲得了系統(tǒng)性的研究成果(Eur.?J.?Med.?Chem.?2018;Acta Pharmacol.?Sin.?2019;J. Med. Chem.?2022;Bioorg. Chem.?2024)。然而,CBP/p300小分子抑制劑會面臨兩個問題:(1)化合物長期暴露會導(dǎo)致耐藥;(2)化合物單獨靶向CBP/p300的HAT或BRD域可能無法完全消除其功能。因此,迫切需要一種新的策略,以獲得更有效的治療。
蛋白降解靶向嵌合體(PROteolysis TArgeting Chimeras,PROTAC)是一種利用小分子來調(diào)節(jié)蛋白水平的靶向蛋白降解技術(shù)。PROTAC分子可以誘導(dǎo)靶蛋白與E3連接酶相互靠近并,使靶蛋白被泛素化,之后被蛋白酶體降解。在本研究中,我們選擇CCS1477作為CBP/p300的配體,沙利度胺作為E3連接酶CRBN的配體,設(shè)計合成了系列CBP/p300 PROTAC分子(圖1)。
通過系統(tǒng)的構(gòu)效關(guān)系研究和生物活性評價,該團(tuán)隊發(fā)現(xiàn)了兩個高活性的具有雙芳香環(huán)Linker的CBP/p300降解劑XYD190和XYD198(圖2)。這兩個降解劑可有效抑制AML細(xì)胞系MV4;11的增殖(IC50分別為1.8 nM和0.9 nM),并以CRBN和蛋白酶體依賴的方式高效地降解CBP和p300蛋白(DC50?< 2?nM)(圖2)。蛋白質(zhì)組學(xué)研究表明,XYD190和XYD198可有效下調(diào)CBP/p300蛋白,并且對其它溴結(jié)構(gòu)域家族和分子膠底物的蛋白水平無明顯影響。在MV4;11異種抑制瘤模型中,XYD190和XYD198可顯著抑制腫瘤的生長(TGI分別為88%和93%)(圖2)。本研究為AML的治療提供了一種采用新的作用機制的更優(yōu)的候選藥物。
廣州健康院許永研究員和張巖副研究員為共同通訊作者,許永課題組博士研究生胡建康、碩士研究生徐鴻瑞和博士研究生吳天幫為本論文的共同第一作者。該研究得到了國家重點研發(fā)計劃,國家自然科學(xué)基金,廣東省基礎(chǔ)與應(yīng)用基礎(chǔ)研究項目,廣州市科技計劃項目,廣東省“一帶一路”聯(lián)合實驗室基金,中科院STS項目,中國博士后科學(xué)基金,廣東省博士后專項的支持。
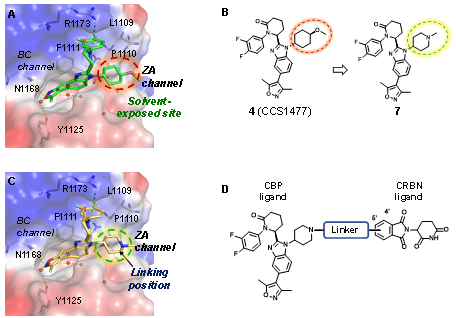
圖1. 靶向CBP/p300的PROTAC降解劑的設(shè)計策略
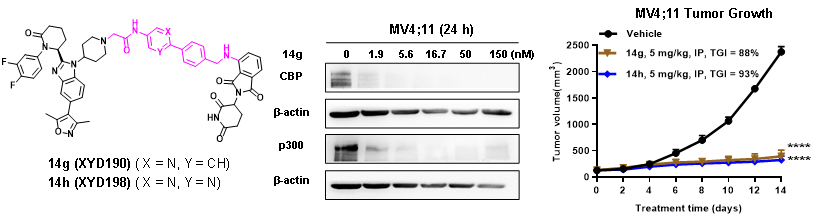
圖2. XYD190和XYD198的結(jié)構(gòu)及活性數(shù)據(jù)
附件下載:

